
Лекарственные препараты — одна из самых сложных категорий в патентной системе. Немногие страны смогли настроить патентную защиту таким образом, чтобы она поддерживала заинтересованность в разработке новых лекарств с одной стороны и не приводила к чрезмерному завышению цен на оригинальные препараты с другой. Если в России патентная система слишком лояльно относится к регистрации новых лекарств и приводит к слишком раннему появлению дженериков, то в США проблема прямо противоположная.
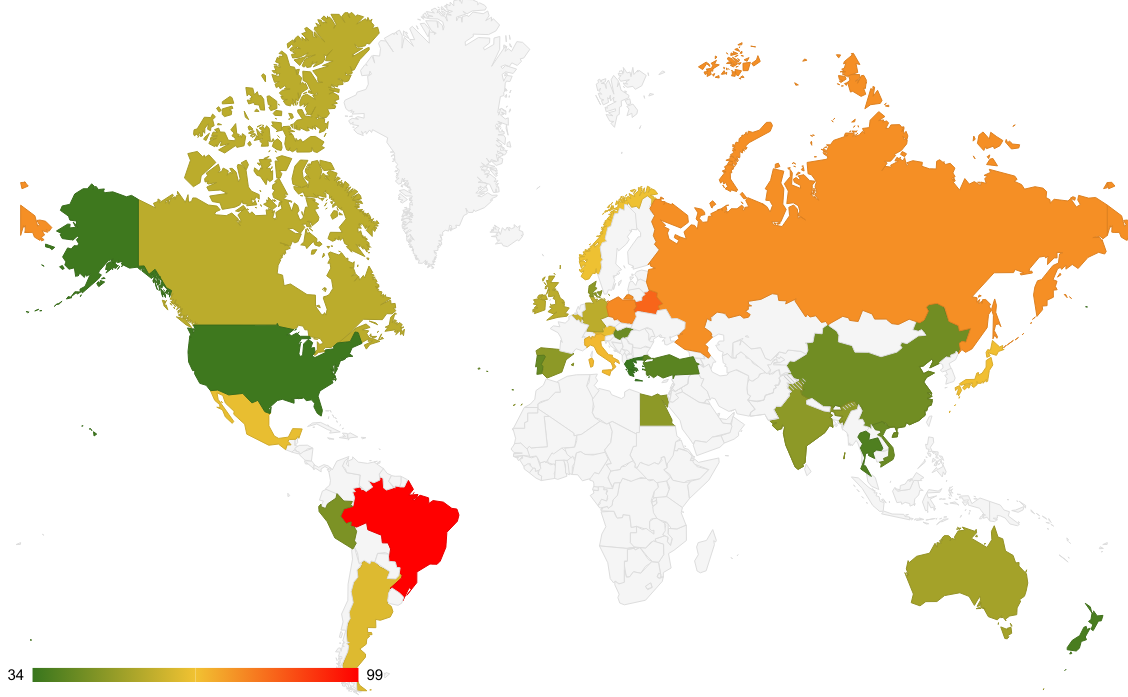
На диаграмме выше отмечено соотношение (в процентах) заявок на патенты к выданным патентам за 2021 год по статистическим данным ВОИС. На этом основании нельзя сказать, что одобряется именно такой процент всех заявок, но данные всё равно хорошо отражают лояльность патентной системы. Из отмеченных на карте стран патентная система США наиболее жёсткая — выданные патенты составляют только 35% от объёма заявок. Другие исследования, пусть и поднимают число одобряемых заявок до 52% (на 2015 год), также подтверждают сложность получения патента в США (в том числе и на лекарства).
Особенности патентования в США
Система интеллектуальной собственности в США в целом сильно отличается от привычной. Это распространяется как на товарные знаки, так и на патенты. Так, регистрация разработки может проходить в два этапа (согласно официальной информации Патентного ведомства США):
Предварительная заявка. Изобретатель заявляет о намерении зарегистрировать разработку, указывая лишь общие характеристики. Описание и формула технического решения может не предоставляться.
Окончательная регистрация. До того, как перейти к этому этапу, разработчик может в течение года проводить различные дополнительные испытания технологии, в том числе с точки зрения коммерческой применимости. На заключительном этапе уже обязательно указывается формула и подробное описание изобретения.
При этом нельзя зарегистрировать препарат, не только повторяющий описанные в других патентах, но и в целом уже раскрытый общественности.
Эксклюзивность — дополнительная система защиты
Одновременно с патентной защитой лекарства в США приобретают так называемую эксклюзивность со стороны Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). То есть после оформления заявки на лекарства в FDA Управление не будет одобрять похожие медикаменты конкурентов. Причём период действия эксклюзивности может не совпадать со временем действия патентной защиты.
Например, в книге запатентованных лекарств, составленной I-MAK (структура, занимающаяся проблемой равного и справедливого доступа к лекарствам), 1275 препаратов не состоят в перечне лекарств с актуальной защитой FDA (в оранжевой или фиолетовой книге) и только 154 препарата находятся под такой защитой.
Согласно официальному сайту, цель существования такой эксклюзивности — баланс между инновациями (новыми препаратами) и широким доступом общественности к лекарствам, возникающим в ходе конкуренции за непатентованные препараты. Фактически такая система позволяет устанавливать первенство среди производителей дженериков. Сроки действия эксклюзивности различаются от типа препарата и могут длиться от 180 дней до 7 лет.
Чрезмерное патентование и завышенные цены
Срок действия патента на лекарство в США составляет 20 лет, если в ходе рассмотрения заявки не было чрезмерно длительных задержек или других условий. В то же время существует понятие вторичного патента — такие разработки раскрывают новые аспекты или вносят усовершенствования в лекарство. По факту такая система позволяет получить на одно и то же по сути лекарство хоть 100 патентов.
Это зачастую приводит к удержанию монополии на рынке и чрезмерному завышению цен (взять хотя бы длящуюся больше века историю с инсулином). В этом отношении показательно исследование I-MAK о десяти самых продаваемых лекарствах в США. Так, среднее количество патентов для каждого из этих 10 лекарств составило 74,1. В среднем 66% патентных заявок было подано уже после получения одобрения FDA, а средний срок патентной защиты для каждого лекарства уже составляет более 40 лет. При этом с момента запуска лекарства цены в среднем увеличились на 212%. Средний прирост цен за последние 5 лет составил 44% и в три раза превысил инфляцию.
Диаграмма с информацией о патентах и росте цен по 9 из 10 самых продаваемых лекарств в США представлена ниже. Также интересно, что согласно отчёту 2021 года о чрезмерно патентуемых лекарствах в США, на оригинальные препараты приходится всего 8% выдаваемых рецептов, но 79% всех расходов.
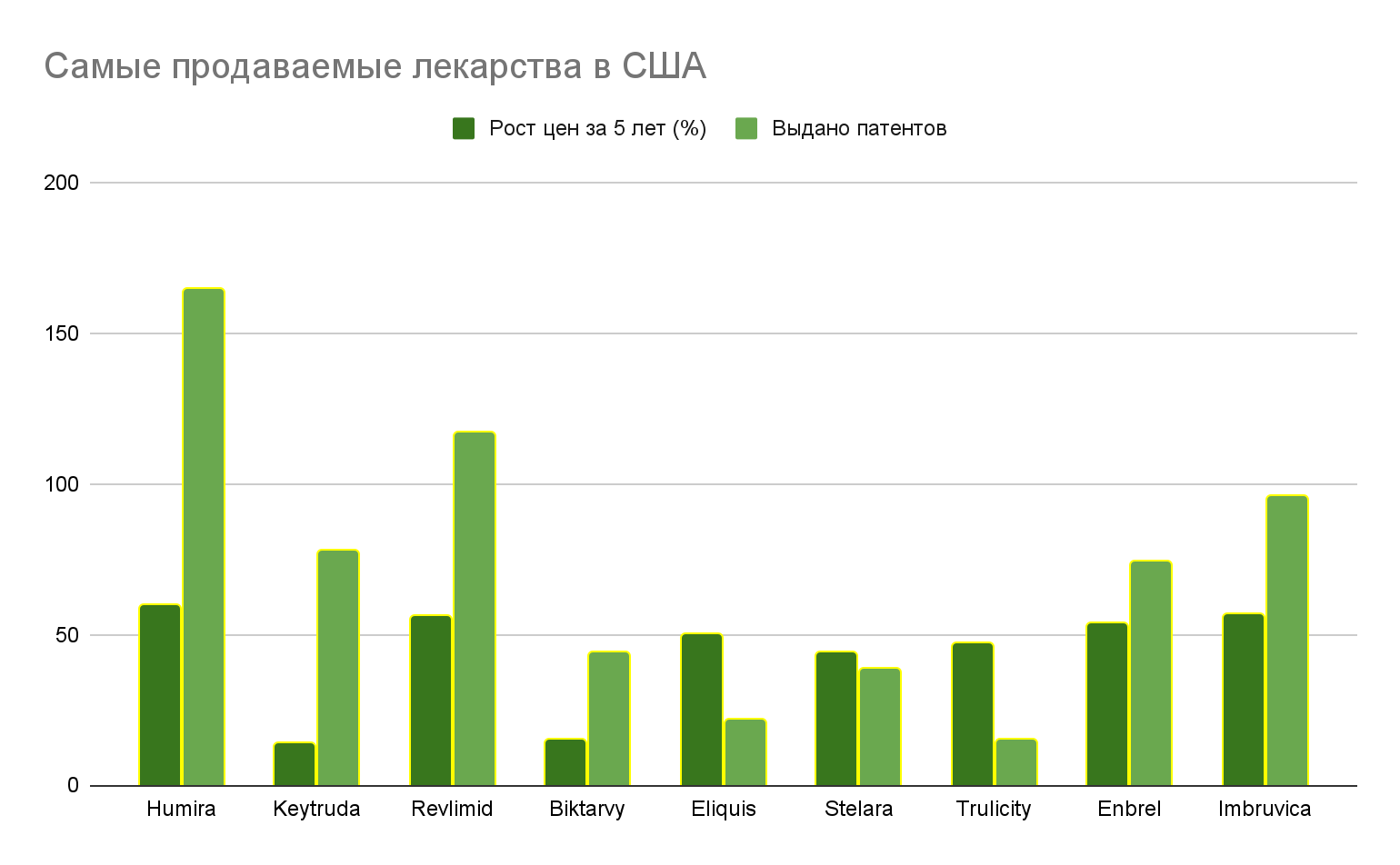
При этом в отчёте 2021 года о чрезмерном патентовании лекарств в США указывается, что это недостаток не патентной системы в целом, а именно ситуации с патентованием лекарств в Америке. Приводятся данные о том, что аналоги трёх самых продаваемых препаратов появились в Европе в среднем на 7.7 лет раньше ожидаемого появления в Соединенных Штатах. По ряду лекарств дженериков всё ещё нет. На всю десятку самых распространённых препаратов при этом в среднем приходится в четыре раза больше патентов в США, чем в Европе.
С другой стороны, без патентной системы производители оригинальных лекарств не смогут коммерчески компенсировать свои расходы. Разные исследования предлагают разные оценки того, сколько стоит не просто разработать, а вывести на рынок новые лекарства. Оценки разнятся от 757 млн до 3,558 млрд долларов.
Изменения законодательства
На рынок патентованных лекарств в США существенно повлияли два закона — О ценовой конкуренции на лекарства и восстановлении срока действия патентов 1984 года и Об изобретениях Америки 2011 года.
Первый, он же Закон Хэтча-Ваксмана, поспособствовал появлению на рынке препаратов-дженериков (повторяющих оригинальные лекарства) в больших количествах и повышению числа их выписывания врачами — с 20% до принятия закона до 80% после. Закон, в частности, упростил прохождение процедур FDA для таких лекарств. Теперь производителям дженериков гораздо проще доказать их «биоэквивалентность» оригинальному препарату (схожесть действия и эффективности). Впрочем, для получения защиты со стороны FDA должно быть доказано одно из следующих условий:
Нет пересечения с действующими патентами;
Препарат совпадает в истекшим патентом;
Производитель не может продавать дженерик, пока действует оригинальный патент;
Производитель считает, что актуальный патент нерелевантен или недействителен.
За счёт третьего условия производители дженериков подготавливают всё к производству и продаже ещё во время действия оригинального патента, и могут реализовывать лекарство совсем без задержек после истечения срока действия патента.
Впрочем, как показывает диаграмма ниже, далеко не всегда аналоги успевают появиться на рынке одновременно с истечением срока действия первичного патента. Так, первичные патенты Revlimid перестали действовать в 2016 и 2019 годах, но почти ⅔ продаж пришлись уже на период после этих событий. Отчасти так произошло потому, что аналоги лекарства должны появится на рынке только в 2023 году.

В то же время четвёртое условие, а также содержание второго значимого закона (Об изобретениях Америки) способствует увеличению патентных споров, так как упрощает процедуру оспаривания патента на лекарственные препараты. Это же вынуждает производителей оригинальных препаратов более пристально следить за возможностью появления новых дубликатов.
Так, разрешать патентные споры, связанные с лекарствами, в США сейчас можно в административном, а не судебном порядке, что гораздо проще и быстрее (по некоторым оценкам производители дженериков добивались хотя бы частичного оспаривания патента в административном порядке в 87% случаев, а при федеральном разбирательстве — в 42%). Примерно в 2015 году производители лекарств обращались в Конгресс с просьбой упразднить административные разбирательства, но не добились своего. Было выявлено, что удовлетворение такой просьбе могло привести к увеличениям затрат здравоохранения США на 1,3 млрд долларов в течение 10 лет.
Борьба с завышенными ценами на препараты ведётся и другими методами. Например, в 2020 году ряд политиков предлагали ограничить производителей лекарств только одним патентом в отношении того или иного препарата. Пока что такая практика не предусмотрена.
Итоги
Патентование лекарств в США имеет ряд преимуществ перед аналогичными системами других стран. В то же время на практике оказывается, что производители оригинальных препаратов всеми силами стараются удержать единоличное право на продажу лекарств, а производители дженериков не всегда способны составить достойную конкуренцию даже после истечения срока первичного патента на лекарство. Всё это приводит к завышенным ценам и новым волнам критики системы патентной защиты в целом.
Дарим скидку 4000 рублей при первом обращении на любую услугу onlinepatent.ru
Промокод: LOVEHABR






